Nguyễn Hoàng Hải, ĐHQGHN
4/1/2025
>**Mục đích**
>Nghiên cứu sự chuyển pha của nước để thấy sự chuyển pha tuân theo ba quy luật cơ bản của Chủ nghĩa duy vật biện chứng.
## Ba quy luật cơ bản của Triết học Mác-Lênin
1. Quy luật thống nhất và đấu tranh của các mặt đối lập.
2. Quy luật sự thay đổi về lượng dẫn đến sự thay đổi về chất.
3. Quy luật phủ định của phủ định.
4. Xem [[Ba quy luật cơ bản]] của Triết học Mác-Lênin.
## Ví dụ: chuyển pha của nước
Thông thường, nước có thể ở một trong ba trạng thái: rắn, lỏng, khí. Xem [[Nước là một chất lỏng]].

Hình 1: Giản đồ pha của nước ở các điều kiện nhiệt độ và áp suất khác nhau. Đường nằm ngang màu đỏ là giản đồ pha tại áp suất khí quyển 1 atm (1 bar). Chúng ta sẽ xem xét chuyển pha ở áp suất này.
### Các khái niệm
1. "Sự vật" xem xét là "trạng thái", còn gọi là "pha" của nước như là tập hợp các phân tử H$_2$O. Ở các điều kiện nhất định, nước có thể ở các trạng thái khác nhau. Trạng thái của nước được đặc trưng bởi các thông số trạng thái $P,V,T,N,E$.
2. Ở đây chúng ta xem xét sự thay đổi của nhiệt độ $T$, các thông số trạng thái khác là ở điều kiện tiêu chuẩn (áp suất khí quyển khoảng 1 atm, xem Hình 1), số lượng phân tử nước là không thay đổi.
3. "Lượng" chính là "nhiệt độ", là đại lượng vật lí vĩ mô mà chúng ta có thể quan sát. "Động năng" của một phân tử nước là đại lượng vật lí vi mô tỉ lệ với nhiệt độ nhờ vào hằng số Boltzmann: $mv^2/2=3kT/2$. Lượng thay đổi tức là nhiệt độ thay đổi, đồng nghĩa với động năng của phân tử nước thay đổi. Chú ý: động năng ở đây là động năng trung bình, thực tế sự phân bố của động năng không đơn giản mà tuân theo phân bố Maxwell-Boltzmann.
4. "Chất" của sự vật mà chúng ta muốn xem xét là gì? Trong vật lí, sự khác biệt giữa các pha được xác định bởi một đại lượng gọi là "tham số trật tự" $\eta$ (order parameter), một khái niệm do nhà vật lí người Nga là Landau đưa ra vào năm 1937. Tham số trật tự mà chúng ta muốn gán cho nước phải có tính chất triết học: xác định nó là nó và phân biệt nó với cái khác.
5. Chúng ta sử dụng tham số trật tự là: hàm phân bố nguyên tử, liên kết hydrogen. Để dễ hiểu, chúng ta sử dụng liên kết hydrogen để làm chất. Cụ thể là thời gian liên kết. Thời gian liên kết của hai phân tử nước ở pha rắn 10 ns, lỏng từ 1 - 5 ns [10], pha khí dưới 0.3 ps.
6. Sự chuyển từ trạng thái này sang trạng thái khác gọi là "sự chuyển pha". Để nghiên cứu chuyển pha, người ta phải tính năng lượng tự do Gibbs. Chuyển pha của nước là chuyển pha loại 1 bởi tham số trật tự là đạo hàm bậc 1 của năng lượng tự do biến đổi đột ngột tại điểm chuyển pha: $v=\partial G/\partial P|_T$. Chú ý: năng lượng tự do Gibbs thay đổi liên tục nhưng đạo hàm bậc 1 của nó thì thay đổi gián đoạn (bước nhảy) ở điểm chuyển pha (Hình 2).
7. Giải thích theo tham số trật tự là cách giải thích vĩ mô. Tuy nhiên tại sao tham số đó lại thay đổi đột ngột (gián đoạn) ở điểm chuyển pha? Chúng ta cần có cách giải thích vi mô để hiểu hơn quá trình vật lí xảy ra. Ba trạng thái rắn-lỏng-khí của nước có sự khác biệt quan trọng: tương tác giữa các phân tử nước. Sự thay đổi tương tác ở các pha khác nhau dẫn đến các tính chất đặc trưng cho các pha là khác nhau. Do đó, tương tác giữa các phân tử chính là chất, là đặc tính để phân biệt các trạng thái của nước.
8. Chất là sự khác biệt giữa các pha:
1. Khí: các phân tử H$_2$O có thể chuyển động tự do, giữa chúng hầu như không có tương tác tức là không có lực hút, lực đẩy. Khi chúng đến gần nhau chúng ta có thể coi gần đúng là chúng va chạm đàn hồi để nhanh chóng rời xa nhau. Chất = phân tử nước chuyển động tự do, không có tương tác.
2. Lỏng: các phân tử nước có tương tác với nhau thông qua liên kết hydrogen nhưng chúng vẫn có thể chuyển động tự do mặc dù không thể chuyển động tự do như trạng thái khí. Một phân tử nước này vừa có dao động tại chỗ vừa có thể thay đổi tương tác với nhiều phân tử nước khác. Do đó, dù có tương tác nhưng nước lỏng vẫn có thể di chuyển để có hình dạng của bình chứa nó. Chất = phân tử nước chuyển động tự do, có tương tác linh động.
3. Rắn: giữa các phân tử nước đá có tương tác nhưng sự tương tác giữa phân tử nước này với phân tử nước khác cố định không thay đổi làm cho nước rắn có hình dạng cố định. Chất = phân tử nước không di chuyển, có tương tác cố định. Nước đá có nhiệt độ khác nhau là bởi động năng của phân tử có được ở dạng dao động xung quanh vị trí cố định.
9. Các mặt đối lập:
1. Lực hút giữa các phân tử nước có được nhờ liên kết hydrogen, là một tương tác lưỡng cực-lưỡng cực (xem [[Liên kết hoá học]]).
2. Lực đẩy đến từ động năng của các phân tử nước. Mặc dù phát biểu trên không hoàn toàn chính xác nhưng với một gần đúng chúng ta có thể coi như vậy.
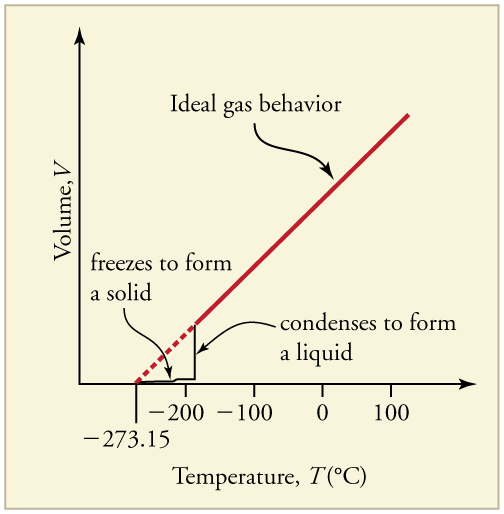
Hình 2: Giản đồ thể tích-nhiệt độ của nước. Đường màu đen cho thấy sự thay đổi đột ngột của thể tích ở điểm chuyển pha.
Xem thêm [[Khái niệm quan trọng của Phép biện chứng]].
### Phân tích triết học
#### Trạng thái cân bằng nhiệt động
Hai mặt đối lập là lực hút và lực đẩy cùng tồn tại trong nước. Chúng có khuynh hướng đối ngược nhau.
Tại một nhiệt độ nào đó, ví dụ ở nhiệt độ phòng, một bình nước ở trạng thái cân bằng nhiệt động. Khi đó lực hút và lực đẩy cân bằng làm cho thể tích của nước không thay đổi.
Ở bề mặt nước, quá trình bay hơi xuất hiện. Khi đó, một số phân tử nước có năng lượng đủ lớn sẽ tách ra khỏi bề mặt để trở thành phân tử khí. Quá trình bay hơi xảy ra ở các nhiệt độ khác nhau, nhưng chỉ xảy ra ở bề mặt lỏng-khí.
#### Chất là gì?
1. Triết học: Chất là bản chất tương đối ổn định của sự vật, quy định sự vật là nó chứ không phải là cái khác. Chất không đồng nhất với một thông số cụ thể, mà là cấu trúc toàn diện và định tính.
2. Vĩ mô: Các tính chất như tính rắn, chảy, khuếch tán, thể tích, độ nhớt, khả năng nén, áp suất hơi, v.v… là những thuộc tính định tính vĩ mô, phản ánh trạng thái của hệ (tức là “chất” vĩ mô), có thể đo được một cách khách quan. Những đặc tính này không thể biến đổi liên tục – tức là có điểm nút → phù hợp với quy luật chuyển hóa lượng – chất.
3. Vi mô: liên kết hydrogen, cụ thể là thời gian tương tác. Rắn: liên kết cố định, thời gian liên kết ≫ ns. Lỏng: liên kết động, thời gian liên kết 1–5 ps. Hơi: không liên kết ổn định, thời gian liên kết < 1 ps.
4. Vi mô: có thể dùng chỉ số tứ diện (tetrahedral order parameter) $q = 1 - \frac{3}{8} \sum_{j=1}^{3} \sum_{k=j+1}^{4} \left( \cos \psi_{jk} + \frac{1}{3} \right)^2$
trong đó $\psi_{jk}$: góc giữa 2 vectơ nối phân tử trung tâm với phân tử nước thứ $j$ và $k$ trong số 4 phân tử lân cận gần nhất, $\cos \psi$ của tứ diện đều là $-1/3$ → khi các góc gần 109.5°, biểu thức đạt giá trị nhỏ → $q \to 1$.
- $q \approx 1$: trật tự gần như hoàn hảo (đá)
- $q \approx 0.5 - 0.8$: trật tự bị nhiễu, như trong nước lỏng
- $q \approx 0$: trật tự hoàn toàn mất, như trong khí
Công thức này đo độ lệch so với hình tứ diện lí tưởng.
5. Cách đo / tính chỉ số tứ diện trong thực nghiệm & mô phỏng
1. Trong mô phỏng động học phân tử (MD):
Với mỗi phân tử nước, tìm 4 lân cận gần nhất (thường xác định bằng khoảng cách ngắn nhất đến nguyên tử oxy).
Tính các góc $\psi_{jk}$ → áp vào công thức trên → tính $q$
Trung bình hóa trên toàn hệ để thu được giá trị trung bình \langle q \rangle
2. Thực nghiệm (gián tiếp):
Không thể đo trực tiếp q bằng kỹ thuật truyền thống.
Nhưng có thể ước lượng từ phổ tán xạ neutron hoặc tia X:
So sánh với phổ từ mô phỏng để suy ra cấu trúc tứ diện.
Phổ góc O–O–O cũng phản ánh góc tứ diện.
#### Thay đổi trạng thái: lượng đổi chất đổi
Giả sử chúng ta tăng nhiệt độ từ thấp đến cao để xem nước đá chuyển pha thế nào.
Khi nhiệt độ tăng lên, các phân tử nước có thêm động năng. Động năng tăng chút ít nước đã vẫn là nước đá. Động năng có thể làm cho phân tử dao động ở vị trí cố định của chúng nhưng chưa đủ làm cho phân tử dịch chuyển sang chỗ khác. Lượng thay đổi chưa dẫn đến thay đổi về chất. Chất ở đây là vị trí cố định của phân tử nước.
Nhiệt độ tăng lớn hơn 0 độ C (điểm nút), phân tử có đủ động năng thoát khỏi vị trí cố định. Giữa các phân tử nước vẫn có tương tác là liên kết hydrogen nhưng một phân tử nước có tương tác với nhiều phân tử nước khác. Ở đây có sự thay đổi về chất: vị trí của phân tử không còn cố định. Phân tử có thể chuyển động tự do mặc dù vẫn có liên kết.
Nếu tiếp tục tăng nhiệt độ tăng chút ít, nước có thể nóng lên nhưng vẫn là nước. Quá trình hoá hơi ở bề mặt diễn ra và tăng theo nhiệt độ. Lượng thay đổi nhưng không có sự thay đổi về chất.
Tiếp tục tăng nhiệt độ đến nhiệt độ sôi 100 độ C (điểm nút), động năng của phân tử thắng được liên kết hydrogen giữa chúng làm cho phân tử nước hoá hơi trong lòng chất lỏng. Ở đây có sự thay đổi về chất: phân tử chuyển động tự do và không có liên kết.
#### Phủ định của phủ định
Chuyển pha thứ nhất: nóng chảy để tạo ra nước lỏng là sự phủ định lần 1.
Chuyển pha thứ hai: hoá hơi để tạo ra hơi nước là sự phủ định lần 2.
Có phủ định lần 3 không? Nếu tiếp tục tăng nhiệt độ, động năng sẽ làm cho các điện tử thoát khỏi sức hút tĩnh điện của hạt nhân và đi ra khỏi nguyên tử. Lúc này nguyên tử bị ion hoá. Phân tử nước H$_2$O không còn tồn tại. Chúng ta thu được một trạng thái gọi là plasma, là hỗn hợp gồm các ion mang điện. Nếu tiếp tục tăng nhiệt độ nữa thì sao? Chúng ta không trao đổi ở đây bởi lúc đó không còn là phân tử nước nữa.
Tính phổ biến của quy luật: cách giải thích về chuyển pha từ cái nhìn vĩ mô dựa trên tham số trật tự và vi mô dựa trên tương tác phân tử có thể được sử dụng để giải thích cho các chất khác.
Nhờ Gemini tinh chỉnh lại:
Xem bài viết của tôi sau đây, bạn hãy:
1. đọc và bổ sung bài viết.
2. tinh chỉnh lại các nội dung với văn phong hàn lâm
3. cập nhật các tài liệu tham khảo.
Kết quả là
## Ba quy luật cơ bản của Phép biện chứng Duy vật trong Triết học Mác-Lênin
Phép biện chứng duy vật, một bộ phận cốt lõi của triết học Mác-Lênin, xem xét thế giới trong sự vận động, biến đổi và phát triển không ngừng. Quá trình này tuân theo các quy luật khách quan, trong đó có ba quy luật cơ bản sau đây [1, 2]:
1. **Quy luật thống nhất và đấu tranh của các mặt đối lập:** Quy luật này chỉ ra nguồn gốc, động lực của sự vận động và phát triển, đó là mâu thuẫn nội tại trong bản thân mỗi sự vật, hiện tượng, hoặc giữa các sự vật, hiện tượng.
2. **Quy luật chuyển hóa từ những thay đổi về lượng thành những thay đổi về chất và ngược lại (Quy luật lượng-chất):** Quy luật này chỉ ra cách thức, hình thức của sự vận động và phát triển, theo đó sự thay đổi về lượng đến một giới hạn nhất định (độ) sẽ dẫn đến sự thay đổi căn bản về chất tại một điểm nút, và ngược lại, chất mới ra đời sẽ tạo ra những thay đổi mới về lượng.
3. **Quy luật phủ định của phủ định:** Quy luật này chỉ ra khuynh hướng của sự vận động và phát triển, theo đó sự vật mới ra đời từ sự vật cũ (phủ định lần một), sau đó lại bị một sự vật mới hơn phủ định (phủ định lần hai). Phủ định của phủ định không phải là sự quay trở lại điểm xuất phát ban đầu một cách đơn thuần mà dường như lặp lại nhưng trên một cơ sở cao hơn, tạo thành hình thái xoáy ốc của sự phát triển.
## Ví dụ Minh họa: Sự Chuyển pha của Nước dưới Góc độ Triết học và Vật lý
Nước (H₂O) là một hợp chất quen thuộc, tồn tại chủ yếu ở ba trạng thái (pha): rắn (nước đá), lỏng (nước) và khí (hơi nước) trong điều kiện thông thường [3]. Sự chuyển đổi giữa các pha này là một ví dụ điển hình có thể được sử dụng để minh họa các quy luật của phép biện chứng duy vật.
_Hình 1: Giản đồ pha của nước ở các điều kiện nhiệt độ và áp suất khác nhau. Đường nằm ngang màu đỏ biểu diễn giản đồ pha tại áp suất khí quyển (khoảng 1 atm). Chúng ta sẽ xem xét sự chuyển pha tại áp suất này._
### Các Khái niệm Vật lý Nền tảng
1. **"Sự vật" và "Trạng thái":** Trong trường hợp này, "sự vật" được xem xét là một lượng xác định các phân tử H₂O. "Trạng thái" hay "pha" của nước (rắn, lỏng, khí) được đặc trưng bởi cấu trúc và tính chất vật lý vĩ mô của hệ. Chúng ta tập trung vào sự thay đổi trạng thái khi nhiệt độ biến đổi, trong khi các thông số khác như áp suất (giả định là 1 atm) và lượng chất được giữ không đổi.
2. **"Lượng" (Quantity):** Trong ví dụ này, "lượng" được biểu thị bởi nhiệt độ (T). Nhiệt độ là một đại lượng vật lý vĩ mô, phản ánh mức độ chuyển động nhiệt của các phân tử. Ở cấp độ vi mô, động năng trung bình của một phân tử tỷ lệ thuận với nhiệt độ tuyệt đối theo hằng số Boltzmann: $\langle E_k\rangle = \frac{1}{2}\langle mv^2\rangle =\frac{3}{2}kT$(đối với khí lý tưởng đơn nguyên tử, và có thể phức tạp hơn đối với phân tử nước). Sự thay đổi về nhiệt độ (lượng) dẫn đến sự thay đổi động năng trung bình của các phân tử nước. Cần lưu ý rằng động năng của các phân tử tuân theo phân bố Maxwell-Boltzmann.
3. **"Chất" (Quality):** "Chất" của sự vật là tổng hợp các thuộc tính khách quan vốn có, phân biệt nó với các sự vật khác. Trong vật lý học, sự khác biệt cơ bản giữa các pha được định lượng hóa bằng một "tham số trật tự" (order parameter, $\eta$), một khái niệm được Lev Landau giới thiệu vào năm 1937 trong lý thuyết về chuyển pha [4, 5]. Tham số trật tự có thể là mật độ, từ độ (trong vật liệu từ), hoặc trong trường hợp này, có thể liên quan đến thể tích riêng hoặc mức độ trật tự cấu trúc. Sự thay đổi đột ngột của tham số trật tự tại điểm chuyển pha đánh dấu sự thay đổi về "chất".
4. **Chuyển pha (Phase Transition):** Là quá trình một hệ nhiệt động chuyển từ một pha này sang một pha khác. Chuyển pha của nước (nóng chảy, hóa hơi) ở áp suất khí quyển là các chuyển pha loại một. Theo phân loại Ehrenfest, chuyển pha loại một được đặc trưng bởi sự gián đoạn (thay đổi đột ngột) của các đạo hàm bậc nhất của năng lượng tự do Gibbs (G) theo nhiệt độ hoặc áp suất. Ví dụ, thể tích $V=(\partial G/\partial P)_T, \quad S=-(\partial G/\partial T)_P,$thay đổi nhảy vọt tại điểm chuyển pha, trong khi bản thân năng lượng tự do Gibbs vẫn liên tục [6, 7].
5. **Bản chất Vi mô của "Chất":** Giải thích dựa trên tham số trật tự là cách tiếp cận vĩ mô. Để hiểu sâu hơn, cần xem xét ở cấp độ vi mô. Sự khác biệt căn bản về "chất" giữa ba pha của nước nằm ở bản chất và cường độ tương tác giữa các phân tử H₂O, cũng như mức độ tự do chuyển động của chúng [8]:
- **Pha Rắn (Nước đá):** Các phân tử H₂O liên kết chặt chẽ với nhau bằng các liên kết hydrogen theo một cấu trúc mạng tinh thể có trật tự cao. Mỗi phân tử dao động quanh một vị trí cân bằng cố định. "Chất" ở đây đặc trưng bởi cấu trúc trật tự, cố định và tương tác mạnh, định hình.
- **Pha Lỏng (Nước):** Các phân tử H₂O vẫn duy trì tương tác đáng kể thông qua liên kết hydro, nhưng cấu trúc kém trật tự hơn và linh động hơn so với pha rắn. Các phân tử có thể trượt lên nhau, di chuyển tương đối tự do, cho phép nước lỏng mang hình dạng của vật chứa. "Chất" đặc trưng bởi sự kết hợp giữa tương tác mạnh và khả năng chuyển động tương đối tự do.
- **Pha Khí (Hơi nước):** Các phân tử H₂O chuyển động gần như hoàn toàn tự do, khoảng cách giữa chúng lớn, và tương tác giữa các phân tử (ngoại trừ các va chạm tức thời) là rất yếu. "Chất" đặc trưng bởi sự chuyển động hỗn loạn, tự do và tương tác phân tử không đáng kể.
_Hình 2: Giản đồ thể tích riêng theo nhiệt độ của nước (minh họa). Sự thay đổi đột ngột của thể tích tại các điểm chuyển pha (0°C và 100°C ở 1 atm) thể hiện sự thay đổi về chất._
### Phân tích Triết học qua Ví dụ Chuyển pha Nước
#### 1. Quy luật Thống nhất và Đấu tranh của các mặt đối lập
Trong hệ nước, hai mặt đối lập cơ bản luôn tồn tại và tương tác:
- **Lực hút giữa các phân tử:** Chủ yếu là liên kết hydrogen, có xu hướng giữ các phân tử lại gần nhau, tạo nên sự cố kết.
- **Chuyển động nhiệt của các phân tử (động năng):** Có xu hướng làm các phân tử chuyển động ra xa nhau, phá vỡ các liên kết.
Sự "thống nhất" của hai mặt đối lập này thể hiện ở chỗ chúng cùng tồn tại trong một thể thống nhất là nước, quy định trạng thái của nước. Sự "đấu tranh" giữa chúng diễn ra liên tục.
- **Cân bằng nhiệt động:** Tại một nhiệt độ nhất định trong một pha (ví dụ, nước lỏng ở nhiệt độ phòng), có một sự cân bằng động giữa lực hút và lực đẩy (biểu hiện qua động năng). Mặc dù các phân tử riêng lẻ có thể bay hơi khỏi bề mặt, trạng thái vĩ mô của nước (ví dụ, thể tích) được duy trì.
- **Sự phát triển do mâu thuẫn:** Khi nhiệt độ thay đổi, sự cân bằng này bị phá vỡ. "Đấu tranh" giữa hai mặt đối lập trở nên gay gắt hơn, dẫn đến sự chuyển đổi sang một trạng thái cân bằng mới, tức là một pha khác. Đây chính là động lực của sự chuyển pha.
#### 2. Quy luật Lượng đổi dẫn đến Chất đổi
Quá trình chuyển pha của nước minh họa rõ nét quy luật này:
- **Giai đoạn tích lũy về lượng:**
- Khi tăng nhiệt độ nước đá từ dưới 0°C lên đến gần 0°C (ở 1 atm), động năng của các phân tử nước tăng lên (lượng đổi). Tuy nhiên, cấu trúc mạng tinh thể của nước đá vẫn được duy trì; nước đá vẫn là nước đá (chất chưa đổi). Các phân tử dao động mạnh hơn quanh vị trí cân bằng nhưng chưa đủ năng lượng để phá vỡ cấu trúc cố định.
- Tương tự, khi đun nóng nước lỏng từ trên 0°C đến gần 100°C, nhiệt độ tăng (lượng đổi), nước nóng lên nhưng vẫn ở trạng thái lỏng (chất chưa đổi).
- **Bước nhảy vọt về chất tại điểm nút:**
- **Tại 0°C (điểm nóng chảy/đông đặc – điểm nút thứ nhất):** Khi lượng nhiệt cung cấp đủ lớn, động năng của các phân tử thắng được một phần lực liên kết trong mạng tinh thể. Cấu trúc rắn cố định bị phá vỡ, nước chuyển từ trạng thái rắn sang trạng thái lỏng. Đây là một sự thay đổi về chất – từ trật tự cố định sang linh động hơn. Tham số trật tự (ví dụ, mật độ) thay đổi đột ngột.
- **Tại 100°C (điểm sôi/ngưng tụ – điểm nút thứ hai):** Khi tiếp tục cung cấp nhiệt, động năng của các phân tử nước lỏng tăng đến mức thắng được gần như hoàn toàn các lực liên kết hydro còn lại. Nước chuyển từ trạng thái lỏng sang trạng thái khí (hơi nước). Đây là một sự thay đổi về chất nữa – từ trạng thái có tương tác đáng kể và thể tích xác định (dù hình dạng không xác định) sang trạng thái các phân tử chuyển động tự do, không có tương tác đáng kể và chiếm toàn bộ thể tích vật chứa.
- **Ngược lại, chất mới quy định lượng mới:** Sau khi chuyển pha, chất mới (ví dụ, nước lỏng) lại có những đặc điểm về lượng (như nhiệt dung riêng, khả năng giãn nở vì nhiệt) khác với chất cũ (nước đá).
#### 3. Quy luật Phủ định của Phủ định
Quá trình chuyển pha của nước cũng có thể được nhìn nhận qua quy luật này:
- **Khẳng định ban đầu:** Trạng thái rắn của nước (ví dụ, nước đá ở dưới 0°C).
- **Phủ định lần thứ nhất:** Khi nhiệt độ tăng đến 0°C và nước đá nóng chảy, trạng thái lỏng được hình thành. Trạng thái lỏng "phủ định" trạng thái rắn bằng cách phá vỡ cấu trúc trật tự, cố định của nó, nhưng vẫn giữ lại một số đặc điểm của sự vật cũ (ví dụ, vẫn là các phân tử H₂O liên kết với nhau, dù lỏng lẻo hơn).
- **Phủ định lần thứ hai (phủ định của phủ định):** Khi nhiệt độ tăng đến 100°C và nước lỏng hóa hơi, trạng thái khí được hình thành. Trạng thái khí "phủ định" trạng thái lỏng bằng cách phá vỡ gần như hoàn toàn các liên kết giữa các phân tử, cho phép chúng chuyển động tự do.
- Kết quả của sự phủ định của phủ định (trạng thái khí) dường như có một số đặc điểm "giống" với trạng thái ban đầu ở một khía cạnh nào đó (ví dụ, sự tự do tương đối của các đơn vị cấu thành, dù ở trạng thái rắn là dao động tại chỗ còn ở khí là chuyển động tự do), nhưng trên một cơ sở mới, cao hơn (mức năng lượng cao hơn, mức độ tự do cao hơn). Quá trình này cho thấy sự phát triển theo hình xoáy ốc.
- **Sự phát triển tiếp theo (khả năng phủ định lần thứ ba):** Nếu tiếp tục tăng nhiệt độ lên rất cao (hàng ngàn độ hoặc hơn), động năng của các hạt sẽ trở nên cực lớn. Các electron có thể bị bứt ra khỏi nguyên tử, và thậm chí các phân tử H₂O có thể bị phân ly thành các nguyên tử hydro và oxy, rồi các nguyên tử này bị ion hóa. Hệ chuyển sang trạng thái plasma – một "biển" các ion dương và electron tự do [9]. Đây là một sự "phủ định" nữa, phủ định cả cấu trúc phân tử H₂O. Trạng thái plasma có những đặc tính hoàn toàn mới so với ba pha thông thường.
### Tính Phổ biến của Quy luật và Kết luận
Cách tiếp cận kết hợp giữa góc nhìn vĩ mô (dựa trên tham số trật tự và các đại lượng nhiệt động) và vi mô (dựa trên tương tác và chuyển động của các phân tử) không chỉ áp dụng cho sự chuyển pha của nước mà còn có thể khái quát hóa cho nhiều quá trình biến đổi chất khác trong tự nhiên. Ví dụ này cho thấy các quy luật cơ bản của phép biện chứng duy vật có khả năng cung cấp một khung khái niệm để phân tích và hiểu các quá trình vận động, biến đổi và phát triển trong cả tự nhiên, xã hội và tư duy.
### Tài liệu tham khảo
1. Engels, F. (1883). _Dialectics of Nature_. (Xem thêm các bản dịch và phân tích hiện đại).
2. Bộ Giáo dục và Đào tạo. _Giáo trình Triết học Mác-Lênin_. (Sử dụng trong các trường Đại học, Cao đẳng Việt Nam).
3. Atkins, P., & de Paula, J. (2014). _Atkins' Physical Chemistry_. Oxford University Press. (Phần về các trạng thái của vật chất và giản đồ pha).
4. Landau, L. D. (1937). On the theory of phase transitions. _Zh. Eksp. Teor. Fiz._, 7, 19-32. (Bài báo gốc, hoặc các sách giáo khoa về Vật lý thống kê trình bày lý thuyết Landau).
5. Goldenfeld, N. (1992). _Lectures on Phase Transitions and the Renormalization Group_. CRC Press.
6. Callen, H. B. (1985). _Thermodynamics and an Introduction to Thermostatistics_. John Wiley & Sons. (Chương về chuyển pha và năng lượng tự do Gibbs).
7. Pathria, R. K., & Beale, P. D. (2011). _Statistical Mechanics_. Academic Press. (Phần về các loại chuyển pha).
8. Eisenberg, D., & Kauzmann, W. (2005). _The Structure and Properties of Water_. Oxford University Press. (Chi tiết về liên kết hydro và các pha của nước).
9. Chen, F. F. (1984). _Introduction to Plasma Physics and Controlled Fusion_. Plenum Press. (Định nghĩa và các tính chất cơ bản của plasma).
10. https://pubs.rsc.org/en/content/articlelanding/2018/sc/c7sc04205a